Longklachten (mede) als gevolg van het gebruik van medicatie en de rol van farmacogenetica
Medicijnen kunnen naast het gewenste effect ook allerlei bijwerkingen veroorzaken. Als deze in de long optreden spreekt men van zogenaamde ‘drug-induced’ longaandoeningen, ofwel een door medicijnen veroorzaakte, toxische long-reactie. Het farmacogenetisch profiel van de persoon kan daarbij een belangrijke rol spelen. Variatie hierin kan de oorzaak zijn dat mensen die hetzelfde geneesmiddel in dezelfde dosis gebruiken, toch een andere werking (effect) of andere bijwerkingen (toxiciteit) van het medicament ervaren.

Men spreekt in de regel liever over medicijnen dan geneesmiddelen, want het is de vraag of alle middelen werkelijk genezen. Medici worden frequent geconfronteerd met verschillen in respons en bijwerkingen van medicijnen, die zich niet louter laten verklaren door dosisverschillen. Veelal hebben patiënten meer dan een aandoening, waardoor diverse medicamenten tegelijkertijd nodig zijn. Soms werken ze elkaar tegen en in andere gevallen kunnen ze elkaars effecten versterken. Het Farmacotherapeutisch Kompas en bijsluiters staan hier vol mee. Binnen de longziekten is de zogenaamde ‘drug-induced’ longaandoening een bekend fenomeen. Hierbij treedt een reactie op in het longweefsel, waardoor het moeilijker wordt om zuurstof op te nemen. Medicijnen en toxische stoffen welke de long via de inademingslucht bereiken kunnen letterlijk adembenemende gevolgen hebben.
Een van de oorzaken waardoor bijwerkingen mogelijk te verklaren zijn, is het genetisch profiel van de patiënt.
De farmacogenetica onderzoekt of verschil in effectiviteit en bijwerkingen middels het genetisch profiel van een patiënt verklaard kan worden. Kennis van farmacogenetica is van groot klinisch belang voor het bepalen van de individuele gevoeligheid van een patiënt voor een medicijn en noodzakelijk voor eenieder die verantwoordelijk is voor het voorschrijven van medicijnen. Polymorfismen in het CYP450 systeem en andere systemen kunnen aanleiding geven tot onbegrepen reacties op medicatie, bijwerkingen of zelfs toxische reacties. Indien een medicus onbegrepen reacties niet kan verklaren, kan de farmacogenetica hier mogelijk een oplossing bieden.
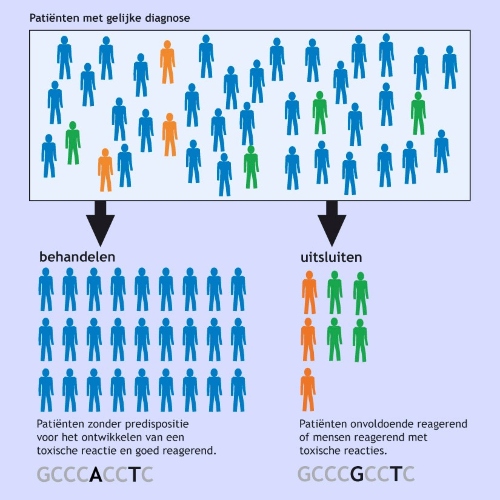
Farmacogenomische kennis toegepast in de medische praktijk. Het is van belang de mensen die reageren op een bepaald geneesmiddel met de gewenste reactie te kunnen onderscheiden van degenen die reageren met een toxische reactie of niet reageren.
Zie verder: O. Bekers. De rol van farmacogenetica bij het voorschrijven van medicatie in de praktijk. ild care today 2009 (link)
Het bijwerkingen centrum Lareb is samen met het ILD Expertisecentrum van de afdeling longziekten van het St. Antonius Ziekenhuis locatie Nieuwegein en de ild care foundation een retrospectief onderzoek gestart met als doel de relatie tussen geneesmiddelen, farmacogenetica en bijwerkingen te onderzoeken in de populatie patiënten met een interstitiële longaandoening (ILD) van het ILD Expertisecentrum. Getracht wordt om met de bevindingen adviezen voor te bereiden voor een voorschrijfbeleid op maat om zo in de toekomst de nog regelmatig niet herkende bijwerkingen te voorkomen.
Hoofdonderzoeker
Dr. Naomi Jessurun, klinisch farmacoloog, Bijwerkingencentrum Lareb
Naomi Jessurun (1973) volgde haar opleiding tot ziekenhuisapotheker in het Meander Medisch Centrum na haar studie farmacie aan de Universiteit van Utrecht. In 2004 begon zij als ziekenhuisapotheker in het Academisch Ziekenhuis Paramaribo, waar zij het Pharmacovigilance Centre voor Suriname startte en contactpersoon was voor de World Health Organization en de Pan American Health Organization voor farmacovigilantie in het Caribische gebied. Sinds 2011 werkt zij bij het Bijwerkingencentrum Lareb en sinds 2019 als hoofd harmonisatie en delen farmacovigilantiedata. Ze heeft ondermeer de Monitor Biologische Geneesmiddelen en de Bijwerkingenmonitor opgezet. De opleiding tot klinisch farmacoloog volgde ze in het Jeroen Bosch Ziekenhuis. Deze opleiding is inmiddels afgerond. Ze is lid van het ild care foundation researchteam en van de adviesraad van de longfibrosepatiëntenvereniging. Tevens is ze bestuurslid van de Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie (KNMP). Op 14 februari heeft ze haar proefschrift getiteld: ‘The metabolization of drugs as a factor in the development of adverse drug reactions’ aan de Rijksuniversiteit Groningen aan de faculteit farmacie, farmacotherapie en farmaceutische zorg succesvol verdedigd. email: n.jessurun@lareb.nl.
contactpersoon was voor de World Health Organization en de Pan American Health Organization voor farmacovigilantie in het Caribische gebied. Sinds 2011 werkt zij bij het Bijwerkingencentrum Lareb en sinds 2019 als hoofd harmonisatie en delen farmacovigilantiedata. Ze heeft ondermeer de Monitor Biologische Geneesmiddelen en de Bijwerkingenmonitor opgezet. De opleiding tot klinisch farmacoloog volgde ze in het Jeroen Bosch Ziekenhuis. Deze opleiding is inmiddels afgerond. Ze is lid van het ild care foundation researchteam en van de adviesraad van de longfibrosepatiëntenvereniging. Tevens is ze bestuurslid van de Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie (KNMP). Op 14 februari heeft ze haar proefschrift getiteld: ‘The metabolization of drugs as a factor in the development of adverse drug reactions’ aan de Rijksuniversiteit Groningen aan de faculteit farmacie, farmacotherapie en farmaceutische zorg succesvol verdedigd. email: n.jessurun@lareb.nl.
Supervisoren
Prof. dr. Aalt Bast, Afdeling Farmacologie en Toxicologie, FHML, UM, Maastricht
Prof. dr. Marjolein Drent, ILD Expertisecentrum, Afdeling Longziekten, St. Antonius Ziekenhuis, Nieuwegein en Afdeling Farmacologie en Toxicologie, FHML, UM, Maastricht
Projectteam
Dr. Ankie Harmsze, hoofd Klinische Farmacie, St. Antonius Ziekenhuis, Nieuwegein
Dr. Coline van Moorsel, hoofd onderzoek, ILD Expertisecentrum, Afdeling Longziekten, St. Antonius Ziekenhuis, Nieuwegein
Prof. dr. Otto Bekers, hoofd Afdeling Klinische Chemie, Centraal Diagnostisch Laboratorium, MUMC, Maastricht
Dr. Petal Wijnen, Afdeling Klinische Chemie, Centraal Diagnostisch Laboratorium, MUMC, Maastricht
Prof. dr. Eugene P. van Puijenbroek, farmacotherapie, epidemiologie en economie RUG, Groningen
Dr. Agnes Kant, directeur Bijwerkingencentrum Lareb



Publicaties
Bast A, Drent M. Altered pharmacology and toxicology during ageing: implications for lung disease. Curr Opin Pulm Med 2022; 28:314–320. doi:10.1097/MCP.0000000000000878.
Drent M, Jessurun NT, Wijnen PA, Bekers O, Bast A. Drug-induced comorbidities in patients with sarcoidosis. Curr Opin Pulm Med 2022; 28:468–477. doi:10.1097/MCP.0000000000000889.
Drent M, Wijnen P, Beker O, Bast A. Grapefruit juice facilitates cortisol replacement therapy: role of CYP3A variant alleles. Arch Clin Med Case Rep 2021; 5 (5): 640-648. doi: 10.26502/acmcr.96550403
Jessurun NT, Drent M, Wijnen PA, Harmsze AM, van Puijenbroek EP, Bekers O, Bast A. Pulmonary toxicity associated with simvastatin: role of pharmacogenetics and drug-gene interactions. Drug Saf 2021; 44(11): 1179-1191. doi.org/10.1007/s40264-021-01105-8.
Geeven IPAC, Jessurun NT, Wasylewicz ATM, Drent M, Spuls IP, Hoentjen F, van Puijenbroek EP, Vonkeman HE, Grootens KP, van Doorn MBA, van den Bemt BJF, Bekkers CL. Barriers and facilitators for systematically registering adverse drug reactions in electronic health records: a qualitative study with Dutch healthcare professionals. Expert Opin Drug Saf 2022; Jan 21. doi: 10.1080/14740338.2022.2020756.
Jessurun NT, Wijnen PA, Bast A, van Puijenbroek EP, Bekers O, Drent M. Tamsulosin associated with interstitial lung damage in CYP2D6 variant alleles carriers. Int J Mol Sci 2020; 21(8):E2770. doi: 10.3390/ijms21082770.
Jessurun NT, Drent M, van Puijenbroek EP, Bekers O, Wijnen P, Bast A. Drug-induced interstitial lung disease: role of pharmacogenetics in predicting cytotoxic mechanisms and risks of side effects. Curr Opin Pulm Med; 2019; Sep;25(5): 468-477. doi: 10.1097/MCP.0000000000000590
Proesmans VLJ, Drent M, Elfferich MDP, Wijnen PAHM, Jessurun NT, Bast A. Self-reported gastrointestinal side-effects of antifibrotic drugs in Dutch idiopathic pulmonary fibrosis patients. Lung 2019; 197: 551–558. doi: 10.1007/s00408-019-00260-1.